Описать ограничения, накладываемые на разработку технологии батарей для потребительской электроники, по меньшей мере, проблематично. Идеальная перезаряжаемая батарея должна обладать противоречивыми свойствами — она должна хранить большое количество энергии, при необходимости безопасно отдавать или поглощать большое ее количество и не должна выделять эту энергию при повреждении. Она также должна быть дешевой, нетоксичной, легкой и масштабируемой.
В результате, батарейные технологии представляют собой компромисс между конкурирующими целями. Современные перезаряжаемые литиевые батареи не являются исключением, хотя их, действительно, можно назвать чудом техники. Без них мобильные устройства не были бы сегодня такими замечательными. Мы не утверждаем, что у вас никогда не было мобильных телефонов со свинцово-кислотной батарей (Motorola 2600 «Bag Phone» был одним таких аппаратов), но, в таком случае, у вас были большие карманы. Также толстый пояс или ... вы носили его в рюкзаке? Ведь, свинец-то тяжелый.

Литиевые аккумуляторы значительно эволюционировали с момента их коммерческого запуска в 1991 году. В начале, при их создании использовались мелкие структуры, покрытых металлическим литием, что имело несколько недостатков, включая потерю емкости ячейки с течением времени, внутренние короткие замыкания и довольно высокий уровень тепловыделения. Для решения этих проблем существовали два основных подхода: использование полимерных электролитов и использование графитовых электродов, содержащих ионы лития вместо использования металлического лития. На основе этих двух подходов были разработаны литий-ионные (литий-ионные) и литий-полимерные (Li-Po) ячейки [1]. С тех пор было разработано много различных химических основ.
Несмотря на большое число химических технологий, литиевые батареи по-прежнему имеют несколько общих параметров, которые очень важны для безопасного и эффективного использования в наших проектах. Хотя этот тип батарей уже знаком многим, но то, что мы рассмотрим сегодня, являются причинами характеристик литиевых батарей и правил, которые регулируют их безопасное использование. Что-то менее мистическое, а больше похоже на науку о материалах.
Емкость: литиевые элементы содержат электроды, которые могут хранить и выделять ионы лития:
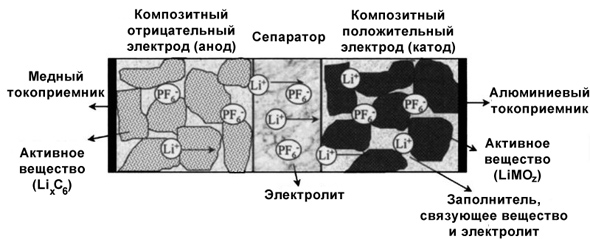
Способность электродов восстанавливать литий является основным фактором, определяющим ёмкость ячейки, поскольку перемещение лития между электродами является причиной протекания тока [3]. Ток, который вы можете непрерывно потреблять в течение одного часа из полностью заряженной ячейки до ее истощения обычно измеряется в миллиампер-часах (мАч). Это значение, как правило, умышленно завышается, особенно недобросовестными компаниями.
Коэффициент C: определяет, как быстро вы можете получить или поглотить ток. Это просто множитель — батарея с коэффициентом 2C может отдавать ток двухкратно превышающий величину заявленной емкости. Например, для батареи емкостью 200 мАч это означает, что вы можете безопасно потребить до 400 мА.
Подвижность лития при перемещении от одного электрода к другому электрод определяет максимальную скорость разряда [3]. Она в основном определяется составом электрода (например, LiFePO4), электролитом и площадью поверхности электродов (больше, значит лучше). Удивительно, что ионы лития не перемещаются далеко — всего на величину порядка микрометра за час, за исключением ячеек с исключительно быстрыми скоростями заряда (и даже тогда на микрометры за минуту).
Стоит отметить, что коэффициент C при зарядке литиевых батарей обычно значительно ниже, чем для разряда (хотя это зависит от конкретной химии, некоторые из них намного быстрее, чем другие). Обратная реакция в этих случаях является просто более медленной по своей природе или чаще приводит к нежелательным побочным реакциям. Помимо нагревания батареи до превышающих норму температур, зарядка с более высоким коэффициентом С может привести к потере постоянной емкости по нескольким причинам, главным образом, из-за разрушения электродов [4].
Пониженное напряжение: нам говорят не допускать, чтобы напряжение литиевых элементов опустилось ниже заданного напряжения (варьируется в зависимости от типа ячейки, но часто это около 3 вольт). Это печально, потому что мы часто «одаряемся» вышедшими из строя литиевыми элементами, регистрируя низкое напряжение, которые было бы неплохо использовать снова, например, в новом фонаре. Однако, это не очень хорошая идея, даже если они способны снова зарядиться.
Оказывается, в элементах в качестве токоприемника обычно используется медная фольга. Когда напряжение падает ниже определенного порога, часть меди на отрицательном электроде начинает растворяться и мигрировать. Вследствие чего, при перезарядке элемента образуются медные наросты там, где их не должно быть.
В лучшем случае, это просто снижает способность элемента принимать ток. Внутреннее сопротивление элемента может повышаться, вызывая значительное тепловыделение во время заряда и разряда. Короче говоря, снижается коэффициент C.
В худшем случае, это приведет к короткому замыканию в ячейке во время зарядки, что приводит к катастрофическим последствиям. Это может произойти немедленно или же через некоторое время. Ниже приведена фотография этого события.
Некоторые (но не все) типы литиевых элементов имеют встроенную схему, которая навсегда отключает элемент, если напряжение падает слишком сильно, для защиты потребителя. Цилиндрические литиевые элементы, такие как 18650, чаще содержат такую схему, чем элементы в виде мешочка.
В любом случае, разумно не допускать чрезмерной разрядки батареи. Любые ячейки, напряжение которых превышает это предельное напряжение могут быть безопасно утилизированы.
Перенапряжение: литиевые элементы могут также быть повреждены, если их заряжать до слишком высокого напряжения. Происходящие реакции зависят от конкретной химии батареи, но обычно твердый металлический литий наносится на отрицательный электрод, что приводит к постоянной потере емкости. Металлический литий является сильно активным и может реагировать с электродом и электролитом с выделением тепла и газа, что может привести к возгоранию.

Другой распространенной реакцией является разложение электролита. Электролит обычно представляет собой органический растворитель, содержащий соли лития, поэтому быть электролизером (подобно соленой воде), образующим газы и твердые вещества [5]. Давление газа может привести к механическому разрушению элемента, а твердые частицы могут способствовать возникновению пористости электродов, уменьшая тем самым их емкость.
Стремительный нагрев: некоторые нежелательные химические реакции в ячейке генерируют тепло и происходят быстрее при более высоких температурах. Станет это причиной возгорания или только выходом и строя элемента, зависит от взаимодействия нескольких факторов, как правило, температуры элемента, физического повреждения и степени заряда [6]. Это хорошо изученный аспект литиевых элементов, описан, например, в этом исследовании, где в реальном времени наблюдались взрывающиеся литиевые элементы. Степень заряда важна, поскольку ток, протекающий через части элемента или посторонний объект (например, гвоздь, прокалывающий элемент) создает локальные точки нагрева. Вот почему батареи, которые вы получаете по почте, могут быть только частично заряжены.
Производственные дефекты: некоторые моменты могут быть выявлены только при серьезном контроле качества. Например, одна из проверенных компаний выявляет металлические примеси между мембранами ячейки, которые могут приводить к коротким замыканиям:

К сожалению, для некоторых компаний принято часто не только экономить на контроле качества, но и заявлять характеристики для своих батарей, находящиеся за гранью фантастики. Как правило, наиболее характерным параметром батареи является емкость. Тем не менее, если вы соблюдаете осторожность в отношении ограничений, касающихся рабочего диапазона напряжений и коэффициента C, батарея будет работать вне зависимости от ее фактической ёмкости.
Вздутие литиевых элементов: не должное обращение с литиевыми элементами, как описано выше, может привести к вздутию, особенно для батарей в виде мешочков. Однако, даже если вы их правильно эксплуатируете, некоторые элементы вздуваются по малопонятным причинам.

Здесь основная опасность заключается в вероятном проколе мешочка элемента чем-то поблизости. Давление, вызванное набухающей литиевой батареей, может также разрушать экраны и клавиатуру. Хорошие производители оставляют небольшие пустоты в корпусе, допуская, тем самым, небольшое набухание. Мы открыли ноутбук со слегка покоробленной клавиатурой, и обнаружили, что эти небольшие пустоты, вероятно, спасли устройство.
Замечание относительно LiFePO4: некоторые достаточно новые элементы LiFePO4 на рынке являются недорогими, заряжаются полностью за 30 минут и вряд ли будут иметь какие-либо химические реакции сопровождающиеся стремительным нагревом. Они хранят около 80% энергии по сравнению с большинством других литиевых элементов, однако выдерживают в 5 раз больше циклов заряда.
Источники:
[1] Vincent, Colin A. 2000. Lithium batteries: a 50-year perspective, 1959–2009. Solid State Ionics. Vol. 134, pp. 159-167.
[2] Arora, P., White, R. E., & Doyle, M. 1998. Capacity Fade Mechanisms and Side Reactions in Lithium‐Ion Batteries. Journal of the Electrochemical Society. Vol. 145 (10), pp. 3647—3667.
[3] Kang, K., Meng, Y. S., Bréger, J., Grey, C. P., & Cedar, G. 2006. Electrodes with High Power and High Capacity for Rechargeable Lithium Batteries. Science. Vol. 311, pp. 977-980.
[4] Ning, G., Haran, B. & Popov, B. N. 2002. Capacity fade study of lithium-ion batteries cycled at high discharge rates. Journal of Power Sources. Vol 117, pp. 160-169.
[5] Pistoia, Gianfranco. 2016. Electric and Hybrid Vehicles: Power Sources, Models, Sustainability, Infrastructure and the Market, Amsterdam, North Holland: Elsevier.
[6] Wang, Q., Ping, P., Zhao, X., Chu, G., Sun, J. & Chen C. 2012. Thermal runaway caused fire and explosion of lithium ion battery. Journal of Power Sources. Vol. 208, pp. 210-224.
[add_ratings]










